- A 100 aranyat érő fű
- Az utolsó gyógyító
- Bodorrózsával a vírusok és baktériumok ellen
- Medvehagyma jótékony hatása
- TOP 7 gyógynövény Influenza ellen
- TOP 8 Immunerősítő gyógynövény
- Mire jó a Bajkáli csucsóka?
- Teakeverékek cukorbetegségre
- Gyömbér mint természetes fájdalomcsillapító
- Univerzális fűszer, mely gyógyít
- Gurmar a cukorbetegek megmentője
- Görögszéna a 2-es típusú cukorbetegség megelőzésére
- Cukorbetegség
Cisztein
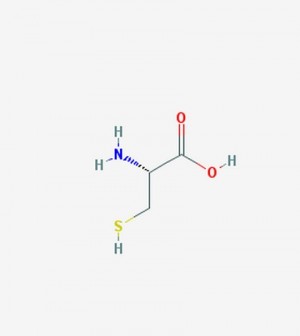
A cisztein (rövidítve Cys vagy C) egy α-aminosav, melynek képlete HO2CCH(NH2)CH2SH. Nem esszenciális aminosav, ami azt jelenti, hogy az emberi szervezet elő tudja állítani. Az UGU és az UGC kodonok kódolják.
Tiolos oldallánccal (R-SH) hidrofil tulajdonsággal rendelkező aminosav. Mivel a tiol oldallánc igen reakcióképes, ezért a cisztein általában kulcsszerepet játszik afehérjék szerkezeti és funkciós elemeként. Nevét oxidált dimerje, a cisztin után kapta. A természetben legelterjedtebb térszerkezetű formája az l-cisztein elnevezésű konformáció.
Bár nem esszenciális aminosav, előfordulhat, hogy bevitele nélkülözhetetlen. Ez főként újszülötteknél, időseknél, vagy egyes metabolikus rendellenességekben szenvedő emberek esetén fordulhat elő. Az emberi szervezetben normális körülmények között megfelelő mennyiségű metioninből szintetizálódik. A cisztein potenciálisan mérgező anyag, ezért a szervezetbe kerülve az emésztőrendszereben cisztinné alakul, mely sokkal stabilabb vegyület. Az emésztőrendszeren és a véráramban cisztin formájában halad át, majd a sejtekhez érve, a sejtbe történő bejutás előtt alakul vissza ciszteinné.
A cisztein a legtöbb, magas fehérjetartalmú élelmiszerben előfordul:
- Állati eredetű: tojás, tej, sajt, joghurt, sertés, kolbász, marha, csirke, pulyka, kacsa, löncshús
- Növényi eredetű: pirospaprika, fokhagyma, vöröshagyma, brokkoli, zab, búzacsíra
Manapság a legolcsóbb, L-cisztein előállítására szolgáló alapanyag az emberi haj, ugyanakkor más szőrök, és tollak is használható e célra. A legnagyobb előállítók Kínábantalálhatók. Bár a legtöbb aminosavat fermentációval már viszonylag régóta elő tudják állítani, az L-cisztein előállításának módját csak 2001-ben, egy német gyár, a Wacker Chemie kísérletezte ki (a folyamatban nincs szükség emberi, vagy állati alapanyagra).
Állatokban a cisztein szintetizálása általában szerinnel kezdődik. A ként a metionin adja, melyet az S-adenozil-metioninen keresztül alakul át homociszteinné. Ezt követően acisztationin béta-szintáz összekapcsolja a homociszteint és a szerint, ezáltal egy aszimmetrikus tioétert, cisztationint képez. A folyamatot a cisztationin gamma-liáz zárja, mely a cisztationint alfa-ketobutiráttá és ciszteinné alakítja.
Baktériumok esetén a folyamat kissé máshogy zajlik: először a szerin O-acetilszerinné alakul a szerin-transzacetiláz segítségével, majd az O-acetilszerint az O-acetilszerin-(tiol)-liáz nevű enzim, kén felhasználásával alakítja tovább ciszteinné. A folyamat acetát felszabadulásával jár.
A ciszteint (főleg az l-ciszteint) az élelmiszer és a gyógyszeripar széles körben alkalmazza. Főként különféle ízek előállítására, például a Maillard-rekció során, amikor a cisztein különféle cukrokkal reagál, végeredményként húsízű anyag termelődik. Ezen kívül pékáruk elkészítésekor is alkalmazzák, ugyanis nagyon kis mennyiségben a tésztához keverve megpuhítja azt, ezáltal az elkészítési idő rövidül. Élelmiszerekben fényesítőanyagként E910 néven, pékárukban alkalmazott adalékanyagként (állagjavítóként) pedig E920 néven alkalmazzák. Napi maximum beviteli mennyisége nincs meghatározva, és nincs ismert mellékhatása.
Egy az öt piacvezető dohánygyár által 1994-ben kiadott jelentésben szerepel, hogy a cisztein egyike azon 599 adalékanyagnak, melyek megtalálhatók a dohánytermékekben, bár a használat pontos indoka nem ismert. Adalékanyagként való felhasználásának két fő oka lehet. Alkalmazásával nő a tüdő nyálkahártyának váladékozása, valamint elősegíti glutation képződését, mely antioxidánsként szolgál, és a dohányzás hatására a glutation szervezetben található mennyisége csökken.